1 van 11
Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: ma 29 jun 2009, 19:42
door Klintersaas
In deze topic vind je modelopgaven chemie die je kunt oplossen ter voorbereiding van de toelatingsproef arts-tandarts. Onder elke vraag kun je het correcte antwoord raadplegen door op de verborgen inhoud te klikken. Heb je een probleem met een vraag of over (de uitwerking van) een bepaalde opgave, klik dan op de link "Stel een vraag over deze oefening" onderaan elke post. Die opent automatisch een nieuw bericht in ons huiswerkforum met de tekst (en eventuele afbeeldingen) van de betreffende opgave. Denk erom dat je in dat bericht beschrijft wat je zelf al geprobeerd hebt om de opgave op te lossen en waar je vast komt te zitten. Enkel om de uitwerking vragen is zinloos en hoe meer je zelf doet, hoe efficiënter we je kunnen helpen. Kijk ook eerst eens rond in het huiswerkforum, want misschien heeft iemand anders al dezelfde vraag gesteld.
Praktische informatie:
- Net als op het toelatingsexamen mag deze tabel gebruikt worden voor alle opgaven.
[attachment=9637:Tabel_sc...tandarts.pdf]
- Het gebruik van een rekenmachine is niet toegestaan.
- Slechts één antwoord is correct.
Veel succes met het toelatingsexamen!
PS: Indien je zelf beschikt over andere modelvragen die je graag met medestudenten wilt delen, stuur dan een persoonlijk bericht naar
Jan van de Velde of
Kravitz.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 17:04
door Klintersaas
1) Bij de volgende omkeerbare reactie:
\(\mbox{A}(aq) + \mbox{B}(aq) \leftrightharpoons 2\ \mbox{C}(aq) + \mbox{D}(aq)\)
meng je 1 mol A met 2 mol B in een volume van 10 L. Na instelling van het evenwicht bij een bepaalde temperatuur vind je als evenwichtsconstante 4. Over de evenwichtsconcentraties kan je met zekerheid zeggen dat:[/i]
\(\left[\mbox{C}\right] = 2 \left[\mbox{D}\right]\)
[/b][/i]\(\left[\mbox{A}\right] = \left[\mbox{B}\right]\)
[/b][/i]\(2 \left[\mbox{C}\right] \left[\mbox{D}\right]= \left[\mbox{A}\right]\left[\mbox{B}\right]\)
[/b][/i]\(4 \left[\mbox{C}\right]^2 \left[\mbox{D}\right]= \left[\mbox{A}\right]\left[\mbox{B}\right]\)
[/b][/i]
Verborgen inhoud
Antwoord A.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 19:28
door Klintersaas
2) De onderstaande grafiek geeft de partiële drukken van gassen in de evenwichtsreactie bij 1000 K:
\(\mbox{H}_2(g) + \mbox{CO}_2(g) \leftrightharpoons 2\ \mbox{H}_2\mbox{O}(g) + \mbox{CO}(g)\)
Op het ogenblik t worden er een of meer veranderingen, telkens apart, op het evenwichtssysteem toegepast, die de verandering van de partiële drukken zoals op de grafiek voor gevolg hebben.
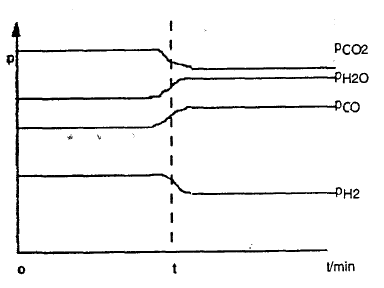
- toevoegen van een katalysator bij constante temperatuur en druk.
- verhogen van de druk bij constante temperatuur.
- toevoegen van argongas bij constante temperatuur.
- verhogen van de temperatuur bij constante druk.
[/i]
Verborgen inhoud
Antwoord D.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 19:45
door Klintersaas
3) Je verwarmt vast \(\mbox{CaCO}_3\) tot 1100 K in een gesloten kolf van een liter. Bij deze temperatuur is de evenwichtsconstante van de dissociatie van calciumcarbonaat:
\(\mbox{CaCO}_3(v) \leftrightharpoons \ \mbox{CaO}(v) + \mbox{CO}_2(g)\)
gelijk aan 0,36. Nu verdubbel je het volume van de kolf bij constante temperatuur en wacht tot het evenwicht zich weer heeft ingesteld. Bij evenwicht is het volgende juist:
- De druk is gedaald tot de helft van de oorspronkelijke druk.
- Het aantal mol \(\mbox{CO}_2\) is verdubbeld.
- De massa \(\mbox{CaCO}_3\) daalde tot de helft van de oorspronkelijke massa.
- Het aantal mol vaste stof verdubbelde ten opzichte van het oorspronkelijke aantal.
[/i]
Verborgen inhoud
Antwoord B.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 19:54
door Klintersaas
4) In welk van de volgende reactievergelijkingen is het reagens dat de rol van zuur speelt met een volle lijn onderstreept?
\(2\ \mbox{H}_2\mbox{SO}_4 + \underline{\mbox{HNO}_3} \longrightarrow \mbox{H}_3\mbox{O}^+ + \mbox{NO}_2^+ + 2\ \mbox{HSO}_4^-\)
\(\underline{\mbox{H}_2\mbox{O}} + \mbox{CO}_3^{2-} \longrightarrow \mbox{OH}^- + \mbox{HCO}_3^-\)
\(\mbox{HCl} + \underline{\mbox{H}_2\mbox{O}} \longrightarrow \mbox{H}_3\mbox{O}^+ + \mbox{Cl}^-\)
\((\mbox{Fe(H}_2\mbox{O)}_6)^{3+} + \underline{\mbox{H}_2\mbox{O}} \longrightarrow (\mbox{Fe(H}_2\mbox{O)}_5\mbox{OH})^{2+} + \mbox{H}_3\mbox{O}^+\)
[/b][/i]
Verborgen inhoud
Antwoord B.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 20:03
door Klintersaas
5) Welk van de volgende stoffen vormen, opgelost in water, een geconjugeerd zuur-basekoppel?
\(\mbox{HClO}_2\)
, \(\mbox{ClO}_2\)
\(\mbox{H}_2\mbox{PO}_4^-\)
, \(\mbox{PO}_4^{3-}\)
\(\mbox{H}_3\mbox{O}^+\)
, \(\mbox{OH}^-\)
\(\mbox{HSO}_4^-\)
, \(\mbox{SO}_4^{2-}\)
[/b][/i]
Verborgen inhoud
Antwoord D.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 20:12
door Klintersaas
6) De ionisatiegraad van azijnzuur in een oplossing van \(\mbox{CH}_3\mbox{COOH}\) in water neemt toe bij toevoeging van volgende stoffen:
\(\mbox{HCl}\)
- zuiver
\(\mbox{CH}_3\mbox{COOH}\)
\(\mbox{H}_2\mbox{O}\)
\(\mbox{NaOH}\)
[/b][/i]
Verborgen inhoud
Antwoord C.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 20:18
door Klintersaas
7) De meest zure oplossing is degene met:
- [H+] = 10-4 M
- [H+] = 0,3 M
- pH = 1,2
- pOH = 5,9
Verborgen inhoud
Antwoord B.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 20:27
door Klintersaas
8) In welk van de volgende oplossingen zal je, door toevoegen van een gelijk volume 0,50 M NaOH, de pH verlagen?
- water
\(0,25\ \mbox{M}\ \mbox{Na}_2\mbox{CO}_3\)
\(0,50\ \mbox{M}\ \mbox{HCl}\)
\(0,60\ \mbox{M}\ \mbox{KOH}\)
[/b][/i]
Verborgen inhoud
Antwoord D.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 20:34
door Klintersaas
9) De evenwichtsconstante voor de autoprotolyse van water bij 298 K is 1,00 · 10-14. De pH van een 1,00 · 10-10 M HCl-oplossing bij 298 K ligt het dichtst bij:
- 10,5
- 10
- 7
- 4
Verborgen inhoud
Antwoord C.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 20:45
door Klintersaas
10) 25,0 mL van een zwak eenwaardig zuur met concentratie 0,10 M wordt getitreerd met een 0,10 M oplossing van NaOH waarbij fenolftaleïne gebruikt wordt om het eindpunt van de titratie te meten. Nu kun je met zekerheid zeggen dat:
- Het volume NaOH dat je moet toevoegen om het equivalentiepunt te bereiken kleiner is dan 0,25 mL.
- De pH bij het equivalentiepunt hoger is dan 7.
- De oplossing kleurloos is na toevoegen van 27,0 mL NaOH.
- Bij het equivalentiepunt \(\left[\mbox{H}^+\right] = \left[\mbox{OH}^-\right]\)
Verborgen inhoud
Antwoord B.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 20:54
door Klintersaas
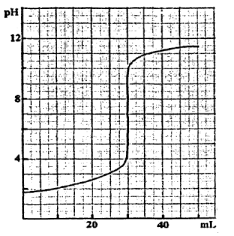
11) Hieronder volgt de titratiecurve van de titratie van 20,0 mL zuur met een base toegevoegd uit een buret. Het gaat om de titratie van:
\(0,015\ \mbox{M}\ \mbox{HCl}\)
met \(0,010\ \mbox{M}\ \mbox{NaOH}\)
\(0,010\ \mbox{M}\ \mbox{HCl}\)
met \(0,015\ \mbox{M}\ \mbox{NaOH}\)
\(0,015\ \mbox{M}\ \mbox{HCl}\)
met \(0,015\ \mbox{M}\ \mbox{NaOH}\)
\(0,050\ \mbox{M}\ \mbox{HCl}\)
met \(0,100\ \mbox{M}\ \mbox{NaOH}\)
[/b][/i]
Verborgen inhoud
Antwoord A.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 02 jul 2009, 22:07
door Klintersaas
12) Oplossingen van \(\mbox{Ag}^+\), \(\mbox{Cu}^{2+}\), \(\mbox{Fe}^{3+}\) en \(\mbox{Ti}^{4+}\) worden onder constante stroom geëlektrolyseerd tot er 0,10 mol van elk metaal is neergeslagen. Voor welk ion duurt dit het langst?
\(\mbox{Ag}^+\)
\(\mbox{Cu}^{2+}\)
\(\mbox{Fe}^{3+}\)
\(\mbox{Ti}^{4+}\)
[/b][/i]
Verborgen inhoud
Antwoord D.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 09 jul 2009, 21:30
door Jan van de Velde
13) Bij de zogenaamde thermietreactie wordt vast Fe2O3 via een reactie met aluminium omgezet tot Al2O3 en ijzer. Veronderstel dat je beschikt over 25,0 g aluminium en 85,0 g di-ijzertrioxide. Gegeven zijn de volgende atoommassa's: O = 16,0; Al = 27,0; Fe = 55,8. Hoeveel gram ijzer kan je maximaal in deze omstandigheden bekomen?
- 29,7 g
- 51,8 g
- 59,5 g
- geen van bovenstaande antwoorden is juist
Verborgen inhoud
Antwoord B.
Stel een vraag over deze oefening.
Re: Modelopgaven chemie voor toelatingsproef arts-tandarts
Geplaatst: do 09 jul 2009, 21:44
door Jan van de Velde
14) Een oplossing van waterstoffluoride in water heeft een concentratie van 20 M. Men wenst te weten hoeveel kg water 1 liter van deze oplossing bevat. Welke combinatie van gegevens heb je nodig om dat probleem op te lossen?
- de dichtheid van de oplossing en de molaire massa van water
- enkel de massapercentagesamenstelling van de oplossing
- de massapercentagesamenstelling van de oplossing en de dichtheid van zuiver water
- de massapercentagesamenstelling van de oplossing en de dichtheid van de oplossing
Verborgen inhoud
Antwoord D.
Stel een vraag over deze oefening.

